
一、肿瘤患者生育力保存的意义与现状
近年来,恶性肿瘤的发病率逐渐上升且呈年轻化趋势。与此同时,随着医疗技术的发展,恶性肿瘤的治疗效果得到明显改善,大约3/4的年轻女性肿瘤患者可被治愈并获得长期生存。但根据研究发现,手术、化疗、放疗将对卵巢功能造成不可逆性损伤,致使许多患者发生不孕。
事实上,约有75%的年轻女性恶性肿瘤患者未来仍有生育愿望。一项对159名恶性肿瘤幸存者的调查问卷显示,26%未接受生育力保存咨询的患者后悔治疗前没有咨询,而84%接受了生育力保存咨询的患者表示满意。当下,肿瘤患者生育力保存成为国内外备受关注和亟待解决的问题。生殖医学的发展,使肿瘤治疗后患者的生育成为可能。
卵巢肿瘤患者生育力保留、保护、保存相辅相成
①生育力保留:如肿瘤治疗的保守性手术(单侧附件切除、双侧卵巢肿物剥除术)、保守性药物治疗(子宫内膜癌大剂量孕激素治疗),在体内原位保留生殖器官,尽量减少手术对于卵巢的损伤。
②生育力保护:如化疗前使用GnRH-a抑制卵巢功能,减少化疗对卵巢功能的损伤(乳腺癌、血液病患者化疗前处理)。
③生育力保存:通过辅助生殖技术获取胚胎、卵母细胞,或妇科手术获得卵巢组织,将其体外保存,待有生育要求时回移体内,完成生育。
卵巢保留性手术后或采取不能完全确定有效性的保护措施后,在下一步治疗前后的卵巢功能更值得关注。
卵巢肿瘤患者生育力保存应视为肿瘤治疗的一部分
目前卵巢肿瘤治疗前生育力咨询情况不乐观。大多数妇科肿瘤患者首先就诊于妇科门诊,直接进行妇科肿瘤的治疗。仅有一小部分患者会被转诊到生殖专家门诊,在妇科治疗前咨询生育力保存。实际上,生育力保存涉及生殖医学和多学科的交叉融合,临床实践中需要妇科医师和生殖科医师及其他科室人员组建MDT团队,充分评估手术适应证、目前的卵巢功能、患者生育需求和婚姻状况、手术对于卵巢功能的潜在风险、生育力保存时机及技术方法,之后再进行个体化治疗。
二、生育力保存技术介绍
2020年ESHRE女性生育力保存指南提出,应向肿瘤患者提供合适的生育力保存咨询。目前公认的首选方案为胚胎或卵子冷冻。卵巢组织冷冻是青春期前儿童保存生育力的主要方法,不推荐用于卵巢低储备或年龄>36岁者。对于接受对性腺有中高风险毒性治疗的患者,当卵子、胚胎冷冻保存不适用时,推荐行卵巢组织冷冻保存。卵母细胞体外成熟是一项创新性技术,但取自卵巢组织的卵母细胞体外成熟仍在实验性阶段。
生育力保存可选择多种方法组合。
目前三项技术保存生育力治疗的妊娠结局
①胚胎冷冻技术:
北京大学人民医院冷冻胚胎复苏后一次临床妊娠率可达50%,活产率90%以上。
优势:该技术应用于肿瘤患者,无恶性细胞再植入的风险。
局限:适用人群范围有限,且不能恢复女性内分泌功能。
②成熟卵母细胞冷冻技术:
据统计每个冷冻卵母细胞的活产率约为5.7%,10个卵母细胞会有真正的活产机会。
优势:通常是非不孕女性,因此可以很容易地对促性腺激素刺激出现反应。适用于单身女性,并且没有恶性细胞再植入的风险。
局限:控制性卵巢刺激(COS)需要10~15天来诱导多个卵泡生长。不能恢复女性内分泌功能,不适用于青春期前女性。
③卵巢组织冷冻技术:
据统计活产率为23%~31%。69%是自然妊娠。获得活产的患者中,进行卵巢冷冻的最小年龄是7岁。超过95%的患者可以恢复内分泌功能,可维持2~7年。
优势:青春期前、不可延迟肿瘤治疗时的唯一选择,肿瘤治疗不受COH激素影响,保守手术顺便留取组织保存,减少组织浪费。可同时恢复内分泌功能。
局限:移植前需对移植片段进行恶性细胞检测,存在恶性细胞重移风险。
生育力保存三大技术的患者条件
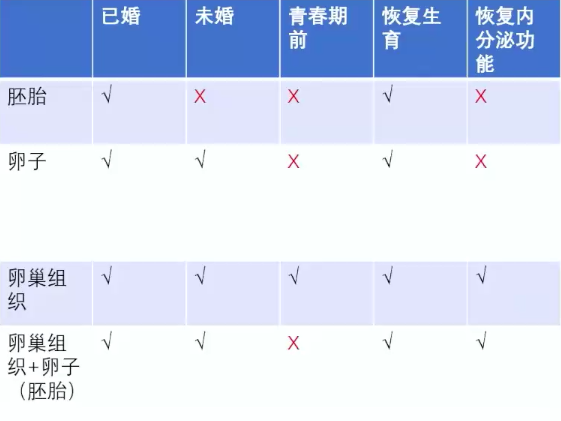
生育力保存三大技术的风险和效果
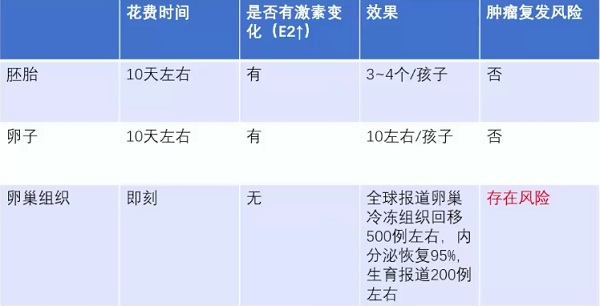
三、卵巢肿瘤患者生育力保存的临床应用现状
1、卵巢良性肿瘤的生育力保存
应用范围:子宫内膜异位囊肿、良性非内异症卵巢肿物、卵巢蒂扭转等均可。
目前妇科手术治疗方案:腹腔镜为主,尽可能保守治疗(肿物剥除术、单侧附件切除术)。
生育力保存建议:双侧卵巢囊肿、复发性囊肿、复发高风险的囊肿,以及卵巢储备低下(年龄> 35岁、卵巢早衰的风险),提供给患者相应的生育力保存的建议。包括COH+卵母细胞或胚胎冷冻,卵巢组织冷冻保存,采集未成熟卵母细胞体外成熟;注意青春期前后的咨询。
2、卵巢交界性肿瘤的生育力保存
目前多数研究表明,在接受治疗的卵巢交界性肿瘤患者中使用COS是安全的,但手术前进行卵母细胞或胚胎保存(进行或不进行COS)仍有争议。可考虑使用芳香酶抑制剂来控制雌激素水平从而降低复发的理论风险。
COH潜在风险:超排高性激素水平、穿刺取卵、囊肿破裂等风险。不建议特殊亚组术前促排(乳头状交界性肿瘤: 复发高风险、雌激素和孕激素受体存在的问题)。
冷冻卵巢组织问题:由于没有使用卵巢刺激,相对安全。存在植入交界性肿瘤细胞的风险。因此,目前并不推荐青春期后女性使用卵巢组织冻存,但是如果COH的结果不佳,大部分卵巢组织被切除,建议进行MDT讨论是否进行卵巢冷冻。
3、卵巢恶性肿瘤的生育力保存
无论是由化疗或手术的治疗方法均会损伤卵巢储备。
化疗已被证明会造成广泛的卵巢损伤。卵巢癌一线化疗方案: 铂类+紫杉醇。铂类化合物通过诱导染色体损伤和DNA交联引起DNA损伤,为性腺毒性、卵巢早衰和闭经中等风险(20%~80%)。顺铂主要影响卵母细胞。紫杉醇导致卵巢衰竭的风险在文献中存在争议,但动物研究发现紫杉醇损害成熟卵母细胞并影响短期生殖潜能。因此,在开始化疗治疗之前,必须完成育力保存。
卵母细胞冷冻:不存在重新植入恶性细胞的风险。但不适用于:不能延迟治疗的女性、青春期前女孩。对于雌激素敏感性的卵巢颗粒细胞肿瘤,推荐使用联合芳香化酶抑制剂进行卵巢轻微刺激。
目前尚无关于卵巢癌患者在卵巢刺激后复发风险的数据。
建议在术中直视下进行取卵,因为经多次经阴道穿刺取卵存在肿瘤破裂种植风险,卵巢癌腹腔内粘连、新生血管,可能会导致相应风险。
卵巢组织冷冻:不会延迟癌症治疗,因为它可以在分期术后立即进行,而且不受月经周期的影响。对于激素依赖性肿瘤来说,它是安全的,因为它不需要COS。但由于卵巢冷冻再植入癌细胞的风险,目前尚无关于卵巢癌患者的卵巢冷冻生殖结局数据。
四、多学科团队下的临床实践具体流程
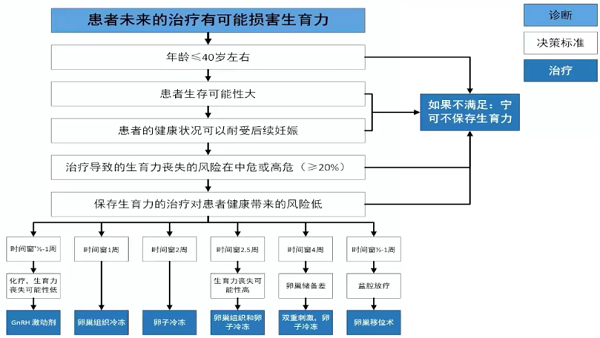
* 时间窗:从患者向生殖中心咨询开始,留给生殖科医生进行生育力保存治疗的时间。
五、挑战与展望
由于妇科肿瘤治疗的特点,建议有生育需求的患者在治疗前或治疗后,均进行生育力的评估,必要时选择适当方式进行生育力保存。
手术、化疗、生育力保存时机的选择,需要MDT团队的讨论和合作。
需要进一步加强临床研究,明确界定各种肿瘤患者生育保存的适应证及最佳临床策略。
加强医疗同行认知,在最佳时机转诊生殖中心咨询,促进多学科协作。
提高社会、肿瘤医生、患者及家属对于生育力保存意义、时机的认知。
技术的进步推动项目的发展。

田莉 教授
北京大学人民医院
主任医师、博士生导师
北京大学人民医院妇产科副主任、生殖中心总负责人
中华预防医学会生育力保护分会常委
中国医师学会生殖医学分会委员
中国中医药促进会生殖委员会副会长
北京医学会生殖医学会委员
北京中西医结合学会生殖医学委员会副主委等
从事生殖医学20余年,有丰富的临床经验及胚胎实验室工作经历,擅长从临床到实验室全面分析管理患者,解决疑难问题。曾参与过985、北京市科委、卫生部行业专项基金、十四五国家重点研发项目等多项科研研究。以第一作者和通讯作者发表SCI及核心期刊论文数十篇。参编多部妇产科及生殖医学著作。




